Produktresumé
Lindring af smerte og inflammation i forbindelse med osteoarthritis hos hund.
Lindring af postoperativ smerte og inflammation i forbindelse med bløddels-, ortopæd- og dentalkirurgi hos hund.
Oral anvendelse.
Osteoarthritis:
Anvend 5 mg pr. kg legemsvægt én gang dagligt som angivet i tabellen nedenfor.
Tabletterne kan anvendes samtidig med eller uafhængig af fodring.
Varighed af behandlingen vil afhænge af det observerede respons. Da feltstudier var begrænset til 90 dage, bør længerevarende behandling overvejes nøje samt være under regelmæssig overvågning af en dyrlæge.
Postoperativ smertelindring:
Anvend 5 mg pr. kg legemsvægt én gang daglig som angivet i tabellen nedenfor i op til 3 dage efter behov. Behandling påbegyndes ca. 2 timer før operation.
Efter ortopædkirurgi kan behandling med samme daglige dosering fortsætte ud over de 3 første dage afhængig af det observerede respons og efter dyrlægens vurdering,
Legemsvægt (kg) | Antal tyggetabletter i forhold til legemsvægt | mg/kg (interval) | |
57 mg | 227 mg | ||
3,0 – 5,5 | 0,5 |
| 5,2 – 9,5 |
5,6 – 7,5 | 0,75 |
| 5,7 – 7,6 |
7,6 – 10 | 1 | 0,25 | 5,7 – 7,5 |
10,1 – 13 | 1,25 |
| 5,5 – 7,1 |
13,1 – 16 | 1,5 |
| 5,3 – 6,5 |
16,1 – 18,5 | 1,75 |
| 5,4 – 6,2 |
18,6 – 22,5 |
| 0,5 | 5,0 – 6,1 |
22,6 – 34 |
| 0,75 | 5,0 – 7,5 |
34,1 – 45 |
| 1 | 5,0 – 6,7 |
45,1 – 56 |
| 1,25 | 5,1 – 6,3 |
56,1 – 68 |
| 1,5 | 5,0 – 6,1 |
68,1 – 79 |
| 1,75 | 5,0 – 5,8 |
79,1 – 90 |
| 2 | 5,0 – 5,7 |
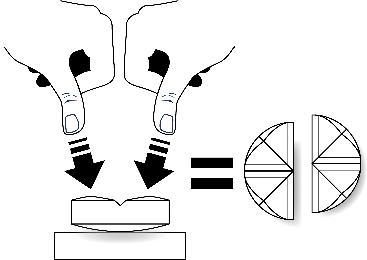
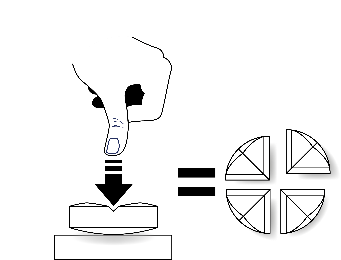
Tabletterne kan deles i 2 eller 4 lige store dele for at sikre en nøjagtig dosering.
|
| |||||||
| Læg tabletten på en plan overflade med delekærven opad og den konvekse (runde) side mod underlaget. | For at dele i 2 lige store dele: Tryk ned på hver side af tabletten med tommelfingrene. | For at dele i 4 lige store dele: Tryk ned i midten af tabletten med en tommelfinger. |
Hund:
Ikke almindelig (1 til 10 dyr ud af 1 000 behandlede dyr): | Opkastning og diarré.1 |
Sjælden (1 til 10 dyr ud af 10 000 behandlede dyr): | Sygdomme i nervesystemet. |
Meget sjælden (<1 dyr ud af 10 000 behandlede dyr, herunder enkeltstående indberetninger): | Hepatiske og renale lidelser.
|
1 Sædvanligvis af forbigående karakter og reversible, når behandlingen ophører.
Hvis bivirkninger som opkastning, gentagen diarré, okkult blod i fæces, pludseligt vægttab, anoreksi, letargi eller ændring af biokemiske parametre for nyre- eller leverfunktion opstår, bør anvendelse af produktet afbrydes, og der bør søges råd hos en dyrlæge. Som for andre NSAID-lægemidler kan alvorlige bivirkninger forekomme, og disse kan i meget sjældne tilfælde være fatale.
Indberetning af bivirkninger er vigtigt, da det muliggør løbende sikkerhedsovervågning af et veterinærlægemiddel. Indberetningerne sendes, helst via en dyrlæge, til enten indehaveren af markedsføringstilladelsen eller dennes lokale repræsentant eller til den nationale kompetente myndighed via det nationale indberetningssystem. Se indlægssedlen for de relevante kontaktoplysninger.
Må ikke anvendes til drægtige og diegivende tæver.
Må ikke anvendes til dyr under 10 uger gamle eller under 3 kg legemsvægt.
Må ikke anvendes til dyr, der lider af gastrointestinal blødning, bloddyskrasi eller blødningsforstyrrelser.
Må ikke anvendes samtidig med kortikosteroider eller andre non-steroide antiinflammatoriske lægemidler (NSAID).
Forudgående behandling med andre antiinflammatoriske lægemidler kan resultere i andre eller øget frekvens af bivirkninger. Der skal derfor være en behandlingsfri periode med sådanne lægemidler på mindst 24 timer, før behandling med veterinærlægemidlet påbegyndes. Ved fastsættelse af den behandlingsfrie periode bør de farmakokinetiske egenskaber for de tidligere anvendte lægemidler tages i betragtning.
Undgå at anvende veterinærlægemidlet samtidig med andre NSAID-lægemidler eller kortikosteroider. Gastrointestinale sår kan forværres af kortikosteroider hos dyr, der behandles med NSAID.
Samtidig behandling med stoffer, der har indvirkning på den renale gennemstrømning, f.eks. diuretika eller angiotensin konverterende enzym hæmmere (ACE-hæmmere), bør medføre klinisk overvågning. Undgå samtidig anvendelse af potentielt nyretoksiske lægemidler, da der kan være forøget risiko for nyretokcicitet. Da anæstetika kan påvirke den renale perfusion, bør anvendelse af parenteral væsketerapi under kirurgi overvejes for at reducere potentielle nyrekomplikationer ved brug af NSAID perioperativt.
Samtidig brug af andre aktive stoffer, der har en høj proteinbinding, kan konkurrere med firocoxibs binding og således føre til toksiske virkninger.
Ingen.