Produktresumé
Til fremkaldelse af midlertidig infertilitet hos raske, fuldstændig, seksuelt modne hanhunde og -ildere.
Hunde:
Subkutan anvendelse.
Den anbefalede dosis er ét implantat pr. hund, uden hensyn til hundens størrelse (se også afsnit 4.4 – Særlige advarsler).
Inden implantationen skal implantationsstedet desinficeres for at undgå infektion. Hvis håret er langt, skal et lille område om nødvendigt klippes.
Veterinærlægemidlet skal implanteres subkutant i det løse skind på ryggen mellem den nederste del af halsen og det lumbale område. Undgå injektion af implantatet i fedt, da frigivelse af den aktive substans kan blive forringet i områder med lav vaskularisering.
1. Fjern luer-lock-hætten fra implantatoren.
2. Sæt aktivatoren på implantatoren ved hjælp af luer-lock-forbindelsen.
3. Løft det løse skind mellem skulderbladene. Indfør kanylen subkutant i hele dens længde.
4. Tryk aktivatorstemplet helt ned og træk samtidigt kanylen tilbage.
5. Tryk på huden på indføringsstedet, medens kanylen trækkes tilbage og oprethold trykket i 30 sekunder.
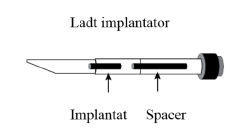
6. Undersøg sprøjten og kanylen for at sikre, at implantatet ikke er blevet tilbage i sprøjten eller kanylen, og at afstandsstykket er synligt. Man kan muligvis føle implantatet in situ.
Gentag indgiften hver 12. måned for at bevare virkningen.
Ildere:
Subkutan anvendelse.
Den anbefalede dosis er ét implantat pr. ilder, uden hensyn til ilderens størrelse.
Inden implantationen skal implantationsstedet desinficeres for at undgå infektion. Hvis håret er langt, skal et lille område om nødvendigt klippes.
Det anbefales at veterinærlægemidlet administreres til ildere under generel anæstesi.
Veterinærlægemidlet skal implanteres subkutant i det løse skind på ryggen mellem skulderbladene. Undgå injektion af implantatet i fedt, da frigivelse af den aktive substans kan blive forringet i områder med lav vaskularisering.
1. Fjern luer-lock-hætten fra implantatoren.
2. Sæt aktivatoren på implantatoren ved hjælp af luer-lock-forbindelsen.
3. Løft det løse skind mellem skulderbladene. Indfør kanylen subkutant i hele dens længde.
4. Tryk aktivatorstemplet helt ned og træk samtidigt kanylen tilbage.
5. Tryk på huden på indføringsstedet, medens kanylen trækkes tilbage og oprethold trykket i 30 sekunder.
6. Undersøg sprøjten og kanylen for at sikre, at implantatet ikke er blevet tilbage i sprøjten eller kanylen, og at afstandsstykket er synligt. Man kan muligvis føle implantatet in situ. Vævslim anbefales til at lukke administrationsstedet om nødvendigt.
Behov for re-implantationer skal baseres på forøget testikelstørrelse og/eller plasmatestosteronniveau samt genoptaget seksuel aktivitet. Se afsnit 4.4 (Særlige advarsler).
Hunde og ildere:
Anvend ikke veterinærlægemidlet, hvis folieposen er i stykker.
Det er ikke nødvendigt at fjerne det biokompatible implantat. Skulle det imidlertid blive nødvendigt at afslutte behandlingen, kan en dyrlæge fjerne implantaterne kirurgisk. Implantater kan lokaliseres ved hjælp af ultralyd.
Hos hunde: En moderat hævelse på implantationsstedet var almindeligt forekommende i 14 dage under studierne af sikkerhed/virkning.
I behandlingsperioden har der været rapporteret om sjældne kliniske effekter; påvirkning af pels (f.eks. hårtab, alopeci, forandringer af hårstruktur), inkontinens, nedreguleringsrelaterede tegn (f.eks. reduceret testikelstørrelse, reduceret aktivitet, vægtøgning). I meget sjældne tilfælde kan en testikel vandre op i annulus inguinalis.
I meget sjældne tilfælde har der været forbigående øget seksuel interesse, øget testikelstørrelse og testikelsmerter umiddelbart efter implantation. Disse tegn forsvandt uden behandling.
I meget sjældne tilfælde har der været rapporteret om forbigående adfærdsændring med udvikling af aggression (se afsnit 4.4 – Særlige advarsler).
Hos mennesker og dyr modulerer testosteron disponering for anfald. I meget sjældne tilfælde (<0,01%) er forbigående tilfælde af anfald rapporteret kort tid efter implantation, selvom der ikke er fastlagt en årsagssammenhæng med implantation af implantat. I nogle tilfælde havde hunden haft epileptiske anfald før implantation eller var diagnosticeret som lidende af epilepsi.
Hos ildere: Forbigående moderat hævelse, pruritus og erythem på implantationsstedet var almindeligt forekommende under de kliniske undersøgelser.
Hyppigheden af bivirkninger er defineret som:
- Meget almindelig (flere end 1 ud af 10 behandlede dyr, der viser bivirkninger i løbet af en behandling)
- Almindelige (flere end 1, men færre end 10 dyr af 100 behandlede dyr)
- Ikke almindelige (flere end 1, men færre end 10 dyr af 1.000 behandlede dyr)
- Sjældne (flere end 1, men færre end 10 dyr ud af 10.000 behandlede dyr)
- Meget sjælden (færre end 1 dyr ud af 10.000 behandlede dyr, herunder isolerede rapporter)
Ingen.
Ingen kendte.
Hunde
Infertilitet opnås fra 8 uger op til mindst 12 måneder efter første behandling. Behandlede hunde skal derfor holdes væk fra tæver i løbetid inden for de første 8 uger efter den første behandling.
Hos to ud af 30 hunde i den kliniske undersøgelse, blev infertilitet først opnået ca. 12 uger efter første behandling, men i de fleste tilfælde var disse hunde ikke i stand til at avle afkom. Hvis en behandlet hund parrer sig med en tæve mellem 8 og 12 uger efter behandling, bør der tages passende forholdsregler for at udelukke risikoen for drægtighed.
Manglende forventet effekt hos hund er ikke almindeligt forekommende (i de fleste af disse tilfælde er der rapporteret manglende reduktion af testikelstørrelse og/eller en tæve er blevet parret). Endelig bestemmelse af manglende behandlingseffekt kunne kun konstateres ved måling af testosteron niveau (en anerkendt surrogatmarkør for fertilitet) I tilfælde af mistanke om manglende behandlingseffekt bør hundens implantat (tilstedeværelse) checkes.
Enhver parring, der finder sted mere end 12 måneder efter indgift af veterinærlægemidlet, kan resultere i drægtighed. Det er dog ikke nødvendigt at holde tæver væk fra behandlede hunde efter re-implantationer i den indledende 8 ugers periode, forudsat at veterinærlægemidlet indgives hver 12. måned.
I enkelte tilfælde kan en behandlet hund miste sit implantat. Hvis der er mistanke om tabt implantat i forbindelse med første implantation, kan dette verificeres ved, at der ikke observeres reduceret omkreds af skrotum eller testosteron-niveau 8 uger efter den dato, hvor implantatet formodes at være tabt, da begge burde reduceres i tilfælde af korrekt implantation. Hvis der er mistanke om tabt implantat i forbindelse med re-implantation efter 12 måneder, kan der observeres en progressiv forøgelse af skrotums omkreds og/eller stigning i plasma testosteron-niveau. I begge tilfælde bør et erstatningsimplantat indgives.
Hundes evne til at avle afkom efter at være vendt tilbage til normale plasmatestosteronniveauer efter indgift af præparatet er ikke blevet undersøgt.
Med hensyn til testosteronniveauer (en anerkendt surrogatmarkør for fertilitet) vendte 68 % af hunde, der fik indgivet ét implantat, i kliniske undersøgelser tilbage til fertilitet indenfor 2 år efter implantation. 95 % af hundene vendte tilbage til normale plasmatestosteronniveauer inden for 2,5 år efter implantation. Imidlertid er de data begrænsede, der viser den fuldstændige reversibilitet af de kliniske virkninger (reduceret testikelstørrelse, reduceret ejakulationsvolumen, reduceret antal spermatozoer og reduceret libido), herunder fertilitet efter 12 måneder eller gentaget implantation. I meget sjældne tilfælde kan den midlertidige infertilitet vare i mere end 18 måneder.
På grund af begrænset mængde data, bør anvendelsen af veterinærlægemidlet hos hunde under 10 kg eller over 40 kg, baseres på en risk-benefit-vurdering foretaget af en dyrlæge. Under kliniske forsøg med Suprelorin 4,7 mg var den gennemsnitlige varighed af suppression af testosteron 1,5 gange længere hos små hunde (< 10 kg) sammenlignet med større hunde.
Kirurgisk eller kemisk kastration kan have uforudsigelig indflydelse (forbedring eller forværring) på aggressiv adfærd. Derfor bør hunde med adfærdsmæssige forstyrrelser og med tilfælde af uhensigsmæssig adfærd over for andre hunde eller andre dyrearter ikke kastreres hverken kirurgisk eller med implantat.
Ildere
Infertilitet (suppression af spermatogenese, reduceret testikelstørrelse, testosteronniveau under 0,1 ng/ml og suppression af moskusagtig lugt) opnås mellem 5 uger og 14 uger efter første behandling i laboratorieomgivelser. Behandlede ildere skal derfor holdes væk fra tæver i løbetid inden for de første uger efter den første behandling.
Testosteronniveau forbliver under 0,1 ng/ml i mindst 16 måneder. Ikke alle parametre for seksuel aktivitet er testet specifikt (seborré, urinmærkning og aggressivitet). Enhver parring, der finder sted mere end 16 måneder efter indgift af veterinærlægemidler, kan resultere i drægtighed.
Behovet for re-implantationer skal baseres på testikelstørrelse og/eller stigning plasmatestosteronniveauet og genoptagelse af seksuel aktivitet.
Reversibilitet af effekten og behandlede hanners evne til efterfølgende at producere afkom er ikke undersøgt. Derfor bør veterinærlægemidlet først anvendes efter at dyrlægen har foretaget en vurdering af risk-benefit forholdet.
I enkelte tilfælde kan en behandlet ilder miste sit implantat. Hvis der er mistanke om at første implantat er tabt, så kan dette verificeres ved, at der ikke observeres reduceret testikelstørrelse eller plasmatestosteronniveau, da begge burde reduceres i tilfælde af korrekt implantation. Hvis der er mistanke om tabt implantat i forbindelse med re-implantation, så kan der observeres en progressiv forøgelse af testikelstørrelse og/eller plasmatestosteronniveau. I begge tilfælde bør et erstatningsimplantat indgives.